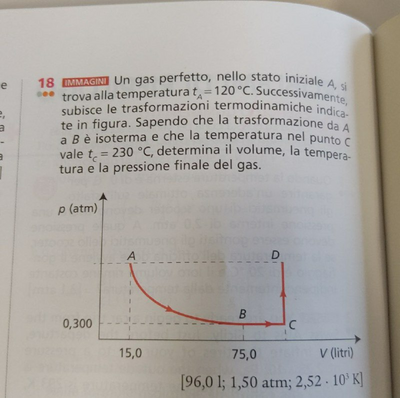
Pa * Va = Pb * Vb; legge delle isoterme; P * V = costante. Ta = Tb = costante.
ta = 120°C;
Ta = 120 + 273 = 393 K, (temperatura assoluta).
tc = 230°C ;
Tc= 230 + 273 = 503 K.
Hai la pressione in atmosfere e il volume in litri o dm^3. Quindi troviamo la pressione in atmosfere.
Pa * 15,0 = 0,300 * 75,0;
Pa = 0,300 * 75,0 / 15,0 = 1,50 atm; (pressione nello stato A).
Da B a C, trasformazione isobara: Volume e temperatura sono proporzionali, è costante il rapporto: V / T = costante.
Pb = Pc = 0,300 atm; pressione costante;
Tb = Ta = 393 K.
Vc / Tc = Vb / Tb;
Vc / 503 = 75,0 / 393;
Vc = 75,0 * 503 / 393 = 96,0 litri.
Da C a D, trasformazione isocora o isovolumica; la pressione aumenta proporzionalmente alla temperatura; Pc = 0,300 atm; Pd = Pa = 1,50 atm.
V costante; Vc = Vd = 96,0 litri;
Pc / Tc = Pd /Td;
0,300 / 503 = 1,50 / Td;
Td = 1,50 * 503 / 0,300 = 2515 K = 2,52 * 10^3 K; (temperatura finale in D).
Coordinate termodinamiche finali del gas:
Pd = 1,50 atm; Vd = 96,0 litri; Td = 2,52 * 10^3 K.
Ciao @federik