Per verificare la legge di Boyle, costruiamo un apparato sperimentale costituito da un contenitore cilindrico di raggio 10 cm e alto 100 cm, riempito con aria. Il tappo ermetico del contenitore è un pistone libero di muoversi lungo tutto l'asse del cilindro. Il contenitore è immerso in un bagno termico che permette di mantenere la temperatura interna costante. Inizialmente la pressione interna è di $1 atm$. In seguito comprimiamo il gas facendo scendere il pistone fino a raggiungere una pressione di $1,3 atm$.
- Calcola l'altezza finale raggiunta dal pistone.
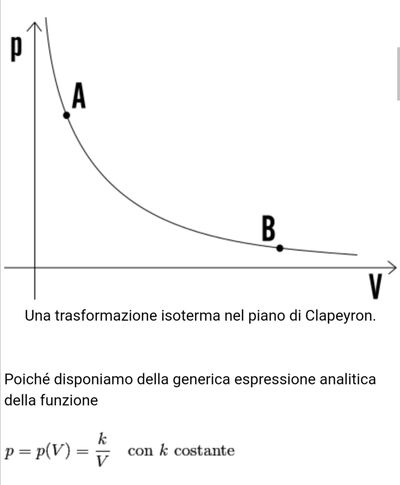
- Rappresenta in un grafico la relazione di proporzionalità inversa fra pressione e volume.
$[77 cm ]$
potreste aiutarmi con questo problema? Grazie mille:)