@gabruie
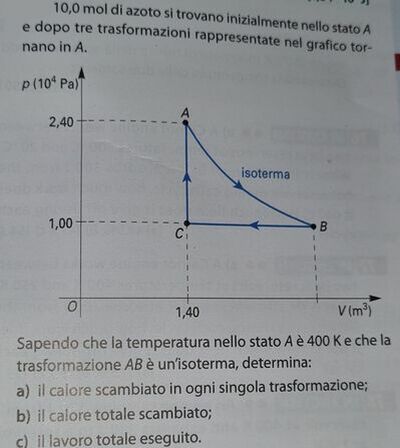
AB isoterma; TA = TB = 400 K;
P * V = costante;
PB * VB = PA * VA;
VB = PA * VA / PB;
VB = 2,40 * 10^4 * 1,40 /1,00 * 10^4 = 3,36 m^3; (volume in B);
QAB = Lavoro;
QAB = n R TA ln(VB / VA) = 10,0 * 8,314 * 400 * ln(3,36 / 1,40) = 29115 J; (calore assorbito AB).
LAB = 29114 J
BC isobara: P costante; TB = 400 K;
QBC = cp * n * (TC - TB);
cp = calore specifico a pressione costante, per un gas biatomico come l'azoto cp = 7/2 * R J/molK.
TC / VC = TB / VB;
TC = TB * VC / VB = 400 * 1,40 / 3,36 = 167 K;
QBC = 7/2 * 8,314 * 10,0 * (167 - 400) = - 67800 J; (QBC, calore ceduto, il gas si raffredda).
LBC = P * Delta V = 1,00 * 10^4 * (1,40 - 3,36) = - 19600 J; (lavoro negativo fatto dall'esterno sul gas)
CA = isocora, il lavoro è 0 J
QCA = cv * n * (TA - TC);
cv = calore specifico a volume costante, per un gas biatomico come l'azoto cv = 5/2 * R J/molK.
QCA = 5/2 * 8,314 * 10,0 * ( 400 - 167) = + 48429 J;
Q ass = 29115 + 48429 = 128243 = 1,28 * 10^5 J; assorbito;
Q ceduto = - 67800 = 6,78 * 10^4 J;
Q ass - Q ceduto = Lavoro del ciclo.
Q totale scambiato= 29115 - 67800 + 48429 = 9744 J = 9,7 * 10^3 J;
Lavoro del ciclo:
L = 29115 - 19600 + 0 = 9515 J = 9,5 * 10^3 J;
Ciao.
@gabruie Ho corretto un po' di errori di calcolo ; grazie a ciccio_aspian