(a) $T_B=517 K ; T_C=96,3 K ;$ b) $P_C=8,59 \cdot 10^5 Pa$
c) $Q_{A B}=0 J ; Q_{B C}=-52,4 kJ ; Q_{C A}=39,0 kJ ;$
d) $\left.L_{A B}=-24,6 kJ ; L_{B C}=0 J ; L_{C A}=11,2 kJ \right]$
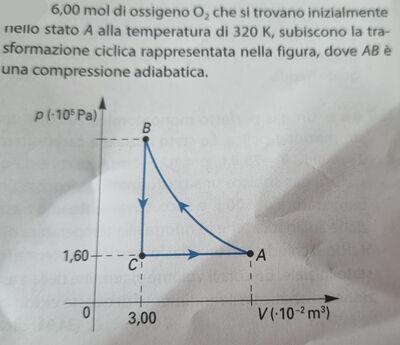
$6,00 mol$ di ossigeno $O _2$ che si trovano inizialmente nello stato $A$ alla temperatura di $320 K$, subiscono la trasformazione ciclica rappresentata nella figura, dove $A B$ è una compressione adiabatica.
Determina:
a) la temperatura in corrispondenza degli stati $B$ e $C$;
b) la pressione nello stato $C$;
c) il calore scambiato durante le singole trasformazioni;
d) il lavoro compiuto durante le singole trasformazioni.