P * V = n R T;
massa molare azoto MM = 28 grammi
n = massa azoto / MM = 15 / 28 = 0,536 mol;
R = costante dei gas; se P è in atm e V è in litri o dm^3 il valore di R è:
R = 0,082 litri atm/(molK); oppure R = 8,31 J(molK) se P in Pascal, V in m^3.
Va = n R Ta / Pa;
Va = 0,536 * 0,082 * 298 / 2,0 = 6,55 dm^3 = 6,6 * 10^-3 m^3.
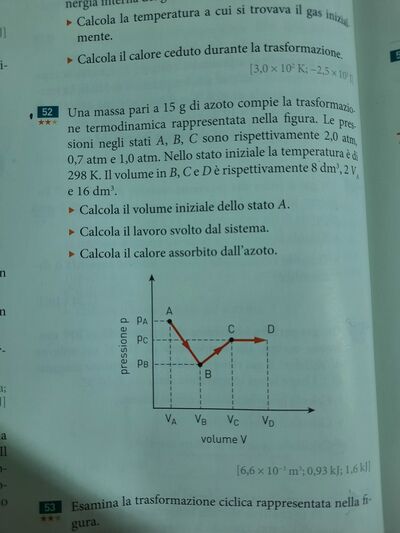
b) il lavoro è l'area sotto il grafico.
La pressione deve essere in Pa, il volume in m^3 per avere il lavoro in Joule.
Vb = 8 dm^3;
Vb - Va = 1,4 * 10^-3 m^3;
A1 = (Pa + Pb) * (Vb - Va) / 2; area trapezio1;
A1 = (2,0 + 0,7) * (1,013 * 10^5 Pa) * (1,4 * 10^-3) / 2 = 191,46 J;
A2 da B a C:
Vc = 2 * Va = 2 * 6,6 * 10^-3 = 13,2 * 10^-3 m^3;
Vc - Vb = (13,2 - 8) * 10^-3 = 5,2 * 10^-3 m^3;
A2 = (Pb + Pc) * (Vc - Vb) / 2;
A2 = ( 0,7 + 1) * (1,013 * 10^5 Pa) * ( 5,2 * 10^-3 ) / 2 = 447,7 J;
A3 è un rettangolo base * altezza.
A3 = Pc * (Vd - Vc) = (1,0 * 1,013 * 10^5 Pa) * (16 - 13,2) * 10^-3 m^3;
A3 = 283,6 J;
Lavoro = A1 + A2 * A3 = 922,8 J = 0,923 kJ:
Calore assorbito:
Q = L + DeltaU;
DeltaU = cv * n * DeltaT;
DeltaU è l'energia che viene assorbita o ceduta dal sistema e non fa lavoro. Dipende dalla variazione di temperatura: Tfinale - T iniziale.
cv = 5/2 R = calore specifico a volume costante per un gas biatomico; R = 8,31 J /molK.
Td = Pd * Vd / (nR) = 1 atm * 16 dm^3 / (0,536 * 0,082) = 364 K
DeltaU = (5/2 R) * 0,536 * (364 - 298) = 20,775 * 0,536 * 66;
DeltaU = 735 J, (variazione dell'energia interna);
Q ass = 923 + 735 = 1658 J = 1,66 * 10^3 J = 1,66 kJ.
Ciao @simone_moraru