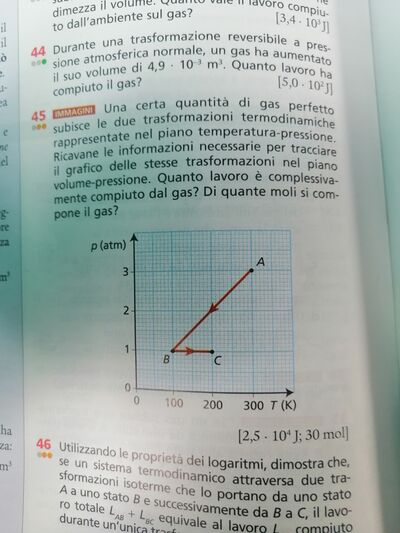
Una certa quantità di gas perfetto subisce le due trasformazioni termodinamiche rappresentate nel piano temperatura-pressione. Ricavane le informazioni necessarie per tracciare il grafico delle stesse trasformazioni nel piano volume-pressione e calcola il lavoro eseguito dal gas. Poi, ricava il numero di moli del gas stesso