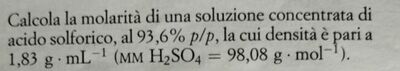Calcola la molarità di una soluzione concentrata di acido solforico, al 93,6\% p/p, la cui densità è pari a $1,83 \mathrm{~g} \cdot \mathrm{mL}^{-1}\left(\mathrm{MM} \mathrm{H}_2 \mathrm{SO}_4=98,08 \mathrm{~g} \cdot \mathrm{mol}^{-1}\right)$.
Per favore mi aiutate grazie